Hiponitröz asit
Hiponitröz asit, H2N2O2 veya HON=NOH formülüne sahip kimyasal bir bileşiktir. Bir nitramid, H2N−NO2 izomeridir.
| Hiponitröz asit | |
|---|---|
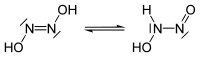 | |
.png.webp) |
.png.webp) |
Diazenediyol | |
N-(Hidroksiimino)hidroksilamin | |
| Tanımlayıcılar | |
| CAS numarası | 14448-38-5 |
| PubChem | 61744 |
| KEGG | C01818 |
| ChEBI | CHEBI:14428 |
| SMILES |
|
| ChemSpider | 55636 |
| 3DMet | B00354 |
| Özellikler | |
| Molekül formülü | H2N2O2 |
| Molekül kütlesi | 62.0282 g/mol |
| Görünüm | beyaz kristal |
| Tehlikeler | |
| Ana tehlikeler | kuru olduğunda patlayıcı |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Hiponitröz asit iki dizi tuz oluşturur: [ON = NO]- anyonunu içeren hiponitritler ve [HON = NO]- anyonunu içeren "asit hiponitritleri".[1]
Yapı ve özellikler
Hiponitröz asidin iki olası yapısı vardır, trans ve cis. Trans-hiponitröz asit, kuruduğunda patlayıcı olan beyaz kristaller oluşturur. Sulu çözeltide, zayıf bir asittir (pKa1 = 7.21, pKa2 = 11.54) ve pH 1–3'te 25 °C'de 16 gün yarı ömrü olan azot oksit ve suya ayrışır:
- H2N2O2 → H2O + N2O
Bu reaksiyon geri dönüşümlü olmadığından, N2O, H2N2O2'nin anhidriti olarak düşünülmemelidir.[1]
Cis asidi bilinmemektedir,[1] ancak sodyum tuzu elde edilebilir.[2]
Üretim
Hiponitröz asit (trans), eterdeki gümüş (I) hiponitrit ve susuz HCl'den hazırlanabilir:
- Ag2N2O2 + 2 HCl → H2N2O2 + 2 AgCl
Spektroskopik veriler, ortaya çıkan asit için bir trans konfigürasyonunu gösterir.[2]
Biyolojik yönler
Enzimolojide bir hiponitrit redüktaz, kimyasal reaksiyonu katalize eden bir enzimdir.[3]
- H2N2O2 + 2 NADH + 2 H+ ↔ 2 NH2OH + 2 NAD+
Kaynakça
- Wiberg, Egon; Holleman, Arnold Frederick (2001). Inorganic Chemistry. Elsevier. ISBN 0-12-352651-5.
- Catherine E. Housecroft; Alan G. Sharpe (2008). "Chapter 15: The group 15 elements". Inorganic Chemistry (3rd ed.). Pearson. p. 468. ISBN 978-0-13-175553-6.
- "Arşivlenmiş kopya". 22 Mart 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Aralık 2019.
