Toluen
Önceden toluol olarak da bilinen toluen tinerin karakteristik kokusuna sahip renksiz, suda çözünmeyen bir sıvıdır. Toluen, bir fenil grubuna bağlı CH3 dan oluşan mono-substituent benzen türevidir. Bundan dolayı toluenin IUPAC sistematik adı metil benzen dir. Toluen bir aromatik hidrokarbondur. Ayrıca TNT(trinitro toluen) patlayıcı madde yapımında kullanılır.
| Toluen | |
|---|---|
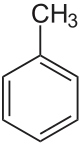 Toluenin molekül yapısı |
 Toluenin top ve çubuk modeli |
Metil benzen | |
Diğer adlar toluen fenil metan toluol Anisen | |
| Tanımlayıcılar | |
| CAS numarası | 108-88-3 |
| PubChem | 1140 |
| DrugBank | DB01900 |
| KEGG | C01455 |
| ChEBI | 17578 |
| RTECS numarası | XS5250000 |
| SMILES |
|
| InChI |
|
| ChemSpider | 1108 |
| Özellikler | |
| Kimyasal formül | C7H8 |
| Molekül kütlesi | 92,14 g mol−1 |
| Görünüm | Renksiz sıvı[1] |
| Koku | tatlı, keskin, benzene benzer kokuda[2] |
| Yoğunluk | 0.87 g/mL (20 °C)[1] |
| Erime noktası |
−95 °C [1] |
| Kaynama noktası |
111 °C [1] |
| Çözünürlük (su içinde) | 0.52 g/L (20 °C)[1] |
| Buhar basıncı | 21 mmHg (20°C)[2] |
| Tehlikeler | |
| GHS piktogramları |    |
| GHS İşaret sözcüğü | Tehlike |
| R-ibareleri | R11, R38, R48/20, R63, R65, R67 |
| H-ibareleri | H225, H361d, H304, H373, H315, H336 |
| P-ibareleri | P210, P240, P301+310, P302+352, P308+313, P314, P403+233 |
| NFPA 704 |
 3
2
0
|
| Parlama noktası | 6 °C [1] |
| Patlama sınırları | % 1.1-%7.1[2] |
| ABD maruz kalma limiti (PEL) |
TWA 200 ppm C 300 ppm 500 ppm (maksimum sınır 10-dakika)[2] |
| Benzeyen bileşikler | |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Endüstriyel özellikleri
Pek polar olmasa da, birçok organik madde için çok iyi bir çözücüdür. Ama tepkime sonrası ortamdan uzaklaştırılması biraz zor olmaktadır.Benzen'in aksine kanserojen olmaması, sanayide de çözücü olarak daha çok tercih edilmesine olanak sağlar. Kuvvetli oksitleyicilerle ve kuvvetli asitlerle şiddetli reaksiyona girer. Üzerindeki metil grubu tolüeni benzene göre 25 kat daha reaktif yapar. Endüstriyel üretimi fosil yakıt kaynaklarından olduğu için nispeten ucuz olarak büyük miktarlarda üretilebilir. Dünyanın yıllık toplam toluen üretimi yaklaşık 12 milyon tondur.
Endüstriyel toluen eldesi
Toluen eldesinin esas (ilk) kaynağı olan fırın gazından toluen eldesinin yerini, gazyağının katalitik bozunması ve buhar ayrımı (destilasyon )sayesinde sıvı (ham) maddelerin piroliz benzinden eldesi, almıştır.
Piroliz benzin, sıvı hidrokarbonların (gazyağı ve petrol benzeri) buhar ayarımı yolu ile ayrılmasından elde edilir. Bu yöntemin tercihi hızla artan bir grafik göstermektedir. Tolueni elde edebilmek için bu ayrılmış likit hidrokarbonlar stabil olamamaları sebebiyle, aromatiklerin çekip ayrılmasından mutlaka önce, hidrojene edilmelidirler. Katalitik bozunma yoluyla toluen eldesinde, aromatik yönden zengin bir hidrokarbon karışımı, 17 bar ile 21 bar arası basınç; 530 °C sıcaklık altında dehidrojenasyon katalizöründen geçirilir.
Fraksiyon yolu ile hafif (kolay uçucu) hidrokarbon gazlarının uzaklaştırılması ardından, aromatiklik yönünden daha da zengin bir distilat elde edilir.
Karışımın destilasyonu
Katalitik Bozunma sonucu elde edilen hidrokarbonlar açısından zengin karşım maddelerin ayrılması için destile edilir
Toluen, bu destilatın azeotropik destilasyondan ya da daha çok kullanılmakta olan (yine bu maddeden) çözücü ekstraksiyonu ile elde edilebilir. Benzen (%99 saflıkta) Toluen (%95 saflıkta) elde edilir. Cyclar denilen ve BP ile UOP tarafından kullanılmakta olan yeni bir proses ise kısaca; Lpg'lerdeki propan ve bütanları aromatiklere dönüştürmeyi ifade eder. Şimdiye dek bu amaçlı kurulan tek fabrika Suudi Arabistanda kurulmuştur. Çok az miktar da olsa toluen, hala taşkömürü karbonizasyonu yöntemiyle, hafif yağ formunda üretilmekteyken, bazı ufak miktarlar ise stiren üretiminde yan ürün olarak geri kazanılmaktadır.
Kullanım alanları
- Genel olarak solvent olarak kullanılır boylarda ve boyaları inceltmek için.
- Birçok kimyasal reaksiyonda reaktant olarak. En genel kimyasal kullanımı benzen ve ksilen eldesidir.
- Plastik (kauçuk) imalatında.
- Mürekkep yapımında.
- Dezenfektanlarda.
- Folluren indikatörü olarak.
- Okside edildiğinde benzaldehit ve benzoik asit gibi çok önemli ara bieşiklere dönüşür.
- Önemli bir karbon kaynağıdır.
- Biyokimyada alyuvarları parçalayıp hemoglobini ortaya çıkrmada.
- Yakıtlarda oktan artırıcı olarak.
- Patlayıcı yapımında TNT (trinitro toluen) ana maddesidir.
Yararlanılan kaynaklar
- Şablon:GESTIS
- ""NIOSH Pocket Guide to Chemical Hazards #0619"". NIOSH. 3 Haziran 2016 tarihinde kaynağından arşivlendi.
