T-şekli moleküler geometri
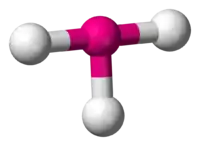
Kimyada, T-şeklindeki moleküler geometri, merkezi bir atomun üç liganda sahip olduğu bazı moleküllerin yapılarını açıklar. Normalde, üç koordineli bileşikler üçgen düzlemsel veya piramidal geometrileri kullanır. T-şekilli moleküllerin örnekleri arasında, halojen triflorürler vardır, örneğin ClF3.[1]
 | |
| Örnek | ClF3 |
|---|---|
| Nokta grubu | C2v |
| Koordinasyon numarası | 3 |
| Bağ açıları | 90°, 180° |
| μ (Polarite) | >0 |

Vsepr teorisine göre üç ligandın ve iki elektron çiftinin merkez atoma bağlanmasıyla, (AXE gösterimde AX3E2) geometri T-şeklinde olur. T-şeklindeki geometri, üç ekvatoral ve iki eksenel ligandlı AX5 moleküllerinin oluşturduğu üçgen çiftpiramit moleküler geometri ile ilgilidir. Bir AX3E2 molekülünde, iki elektron çifti alt ve üst olmak üzere iki ekvatoral pozisyonlarda bulunur ve üç ligand atomu da iki eksenel pozisyonda bulunur. Üç atom, merkezi atomun bir tarafına 90° açıyla bağlanır ve T-şeklini oluşturur.[2]
Trifloroksenat (II) anyonu, XeF3- VSEPR kuralına göre altı elektron çiftinin için oktahedral olarak dizildiği, üç ligandın ve üç yalın elektron çiftinin mer veya T- şekilli dizildiği ilk örnek olarak incelenmiştir.[3] Bu anyon gaz fazında tespit edilmiş olmasına rağmen, çözelti içerisinde sentezlenme girişimleri ve deneysel yapı tespiti başarısız olmuştur. Bir hesaplamalı kimya çalışması, en küçük F-Xe-F bağ açısının, T- şeklinde bir geometride sanıldığı gibi 90° yerine 69° ile çarpık bir düzlemsel Y-şekilli geometrisine sahip olduğunu göstermiştir.[3]
Ayrıca bakınız
Kaynakça
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Oxford: Butterworth-Heinemann. ISBN 978-0-7506-3365-9.
- Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (2nd ed.). Prentice Hall. p. 47. ISBN 978-0-13-039913-7.
- Vasdev, Neil; Moran, Matthew D.; Tuononen, Heikki M.; Chirakal, Raman; Suontamo, Reijo J.; Bain, Alex D.; Schrobilgen, Gary J. (2010). "NMR Spectroscopic Evidence for the Intermediacy of XeF−3 in XeF2/F− Exchange, Attempted Syntheses and Thermochemistry of XeF−3 Salts, and Theoretical Studies of the XeF−3 Anion". Inorg. Chem. 49 (19): 8997–9004. doi:10.1021/ic101275m. PMID 20799721 13 Mayıs 2019 tarihinde Wayback Machine sitesinde arşivlendi.
