Flavonoid
Flavonoidler (veya biyoflavonoidler) (Latince flavus kelimesinden gelen sarı) bitki ve mantar sekonder metabolitlerinin bir sınıfıdır.
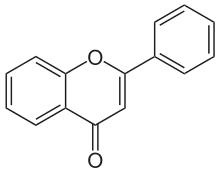
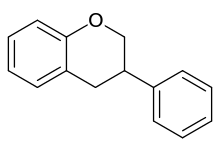
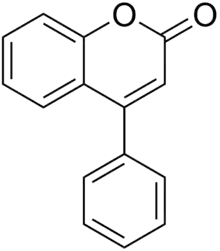
Kimyasal olarak, flavonoidler, iki fenil halkası (A ve B) ve bir heterosiklik halkadan (C) oluşan 15 karbonlu bir iskeletin genel yapısına sahiptir. Bu karbon yapısı C6-C3-C6 olarak kısaltılabilir. IUPAC terminolojisine göre[1][2] şu şekilde sınıflandırılabilirler:
- flavonoidler veya biyoflavonoidler
- 3-fenilkromen-4-on (3-fenil-1,4- benzopirron ) yapısından türetilmiş izoflavonoidler
- 4-fenilkumarin (4-fenil-1,2- benzopirron ) yapısından türetilen neoflavonoidler
Yukarıdaki üç flavonoid sınıfının hepsi keton içeren bileşiklerdir ve bu nedenle antoksantinlerdir (flavonlar ve flavonoller). Bu sınıf ilk olarak biyoflavonoid olarak adlandırıldı. Flavonoid ve bioflavonoid terimleri, keton olmayan polihidroksi polifenol bileşiklerini tanımlamak için daha geniş bir anlamda kullanılmıştır.Flavonoid omurgasındaki üç halkaya genellikle A, B ve C halkası denir. A halkası genellikle bir floroglusinol grubu içerir.
Biyosentez
Flavonoidler, bir amino asit olan fenilalaninin, 4-kumaroil-CoA üretmek için kullanıldığı, fenilpropanoid metabolik yolu ile sentezlenebilir.
Bitkilerde flavonoidlerin fonksiyonları
Flavonoidler, birçok işlevi yerine getirmek için bitkilerde yaygın olarak bulunur. Flavonoidler, çiçeklenme için en önemli bitki pigmentleridir ve tozlanmaya yardımcı hayvanları çekmek için tasarlanmış yapraklarda sarı veya kırmızı-mavi pigmentleri üretir. Daha gelişmiş bitkilerde flavonoidler, UV filtrasyonu, simbiyotik azot fiksasyonu ve çiçek pigmentasyonunda rol oynar. Ayrıca kimyasal uyarıcı, fizyolojik düzenleyici ve hücre döngüsü inhibitörü olarak da işlev görebilirler. Konak bitkinin kökü tarafından salgılanan flavonoidler, bezelye, fasulye, yonca ve soya gibi baklagillerle simbiyotik ilişki kuran Rhizobia'ya yardımcı olur. Toprakta yaşayan Rhizobia, flavonoidleri algılayabilir ve bu da konak bitki tarafından, kök kıllarının deformasyonu, iyon akıları ve kök nodülünün oluşması gibi çeşitli hücresel tepkilere yol açabilen nod faktörlerinin salgılanmasını tetikler. Ek olarak, bazı flavonoidler, bitki hastalıklarına neden olan organizmalara karşı inhibitör aktiviteye sahiptir, örn. Fusarium oxysporum.[3]
Alt gruplar
Çeşitli bitkilerden 5000'den fazla doğal olarak oluşan flavonoid karakterize edilmiştir. Kimyasal yapılarına göre sınıflandırılmışlardır ve genellikle aşağıdaki alt gruplara ayrılırlar[4]:
Antosiyanidinler
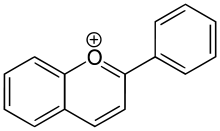
Antosiyanidinler antosiyaninlerin aglikonlarıdır; flavilyum(2-fenilkromenilyum) iyon yapısını kullanırlar
- Örnekler: Siyanidin, Delfinidin, Malvidin, Pelargonidin, Peonidin, Petunidin
Antoksantinler
Antoksantinler iki gruba ayrılır[5]:
| Grup | İskelet Yapısı | Örnekler | |||
|---|---|---|---|---|---|
| Açıklama | Fonksiyonel gruplar | Yapısal formül | |||
| 3-hydroksil | 2,3-dihidro | ||||
| Flavon | 2-fenilkromen-4-on | ✗ | ✗ | 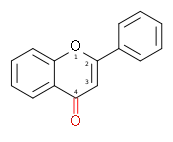 |
Luteolin, Apigenin, Tangeritin |
| Flavonol or 3-hydroksiflavon |
3-hydroksi-2-fenilkromen-4-on | ✓ | ✗ | 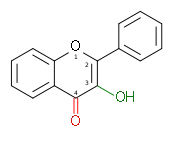 |
Kuersetin, Kemferol, Mirisetin, Fisetin, Galangin, İzorhamnetin, Pachypodol, Rhamnazin, Piranoflavonoller, Furanoflavonoller |
Flavanonlar
Flavanonlar
| Grup | İskelet Yapısı | Örnekler | |||
|---|---|---|---|---|---|
| Açıklama | Fonksiyonel gruplar | Yapısal formül | |||
| 3-hydroksil | 2,3-dihidro | ||||
| Flavanonlar | 2,3-dihidro-2-fenilkromen-4-on | ✗ | ✓ | 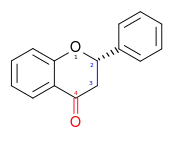 |
Hesperetin, Naringenin, Eriodictyol, Homoeriodictyol |
Flavanonoller
Flavanonoller
| Grup | İskelet Yapısı | Örnekler | |||
|---|---|---|---|---|---|
| Açıklama | Fonksiyonel gruplar | Yapısal formül | |||
| 3-hidroksil | 2,3-dihidro | ||||
| Flavanonoller veya 3-Hidroksiflavanon veya 2,3-dihidroflavonol |
3-hidroksi-2,3-dihidro-2-fenilkromen-4-on | ✓ | ✓ | 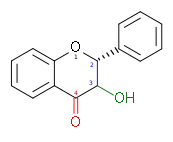 |
Taksifolin (veya Dihidrokuersetin), Dihidrokemferol |
Flavanlar
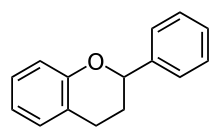
Flavan-3-oller (flavanoller), flavan-4-oller ve flavan-3,4-diolleri içerir.
| İskelet yapısı | Ad |
|---|---|
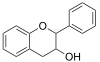 |
Flavan-3-ol (flavanol) |
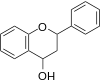 |
Flavan-4-ol |
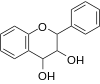 |
Flavan-3,4-diol (lökosantosiyanidin) |
- Flavan-3-oller (flavanoller)
- Flavan-3-ols
- Örnek: Kateşin (C), Gallokatekol (GC), Epigallokateşin Gallat (Cg), Gallokateşin 3-gallat (GCg), Epikateşinler (EC), Epigallokateşin (EGC), Epikateşin 3-gallat (ECg), Epigallokateşin 3-gallat (EGCg)
- Teaflavin
- Örnek: Teaflavin-3-gallat, Teaflavin-3'-gallat, Teaflavin-3,3'-digallat
- Thearubigin
- Proantosiyanidinler, flavanollerin dimerleri, trimerleri, oligomerleri veya polimerleridir.
İzoflavonoidler
- İzoflavonoidler
- İzoflavonlar -fenilkromen-4-one iskelet yapısındanır(2. karbon üzerinde hidroksil grubu olmadan).
- Örnek: Genistein, Daidzein, Glycitein
- İzoflavanlar
- İzoflavandioller
- İzoflavenler
- Coumestanlar
- Pterocarpanlar
Diyet kaynakları



Flavonoidler (özellikle kateşinler gibi flavonoidler) insan diyetinde en yaygın bulunan polifenolik bileşikler grubudur ve her bitkide bulunurlar.[6] Kuersetin gibi biyoflavonoidler olan flavonoller de her yerde bulunur, ancak daha az miktarlarda bulunurlar. Yüksek flavonoid içerikli yiyecekler arasında maydanoz, soğan, yaban mersini ve diğer yemişler, siyah çay, yeşil çay ve oolong çayı, muz, bütün narenciyeler, Ginkgo biloba, kırmızı şarap, karabuğday ve bitter çikolata (kakao içeriği %70 veya daha fazla).[7]
Yaban Mersini
Yaban Mersini Yaban mersini , antosiyanidinlerin diyet kaynağıdır.[8][9]
Narenciye
Narenciye flavonoidleri hesperidin (flavanon hesperetin glikozidi), kuersitrin, rutin (flavonol kuersetin'in iki glikozidi) ve flavon tangeritini içerir.
Kakao
Flavonoidler doğal olarak kakaoda bulunur , ancak acı olabildikleri için genellikle çikolatadan , hatta bitter çikolatadan çıkarılırlar.[10]
Araştırmalar
Her ne kadar flavonoidlerin potansiyel sağlık yararları üzerine devam eden araştırmalar olsa da, ne Amerika Gıda ve İlaç İdaresi (FDA) ne de Avrupa Gıda Güvenliği Otoritesi (EFSA) flavonoidler için herhangi bir sağlık iddiasını onaylamadı veya herhangi bir flavonoidi farmasötik ilaç olarak onaylamadı.[14][15][16]
In vitro
Flavonoidlerin in vitro çalışmalarda çok çeşitli biyolojik ve farmakolojik aktivitelere sahip olduğu gösterilmiştir. Örnekler arasında; anti-alerjik,[17] anti-enflamatuar,[17][18] antioksidan,[18] anti-mikrobiyal (antibakteriyel,[19][20] antifungal,[21][22] ve antiviral[21][22]), antikanser,[18][23] ve anti-diyabet aktiviteleri.[24] Flavonoidlerin ayrıca topoizomeraz enzimlerini inhibe ettiği[25][26] ve in vitro çalışmalardaAkut lenfoblastik lösemi 1(MLL) genindeki DNA mutasyonlarını indüklediği gösterilmiştir.[27] Bununla birlikte, yukarıdaki vakaların çoğunda in vivo veya klinik araştırma yapılmamıştır ve bu aktivitelerin insan sağlığı üzerinde herhangi bir yararlı veya zararlı etkisi olup olmadığını söylemek mümkün değildir. Daha derinlemesine araştırılan biyolojik ve farmakolojik aktiviteler aşağıda açıklanmaktadır.
Antioksidan
Linus Pauling Enstitüsü ve Avrupa Gıda Güvenliği Otoritesi'nde yapılan araştırmalar, flavonoidlerin insan vücudunda (% 5'ten az) zayıf bir şekilde emildiğini, emilenlerin çoğunun hızlı bir şekilde metabolize edildiğini ve atıldığını göstermektedir.[16][28][29] Bu bulgular flavonoidlerin ihmal edilebilir sistemik antioksidan aktiviteye sahip olduğunu ve flavonoid açısından zengin gıdaların tüketiminden sonra görülen kanın antioksidan kapasitesindeki artışın doğrudan flavonoidlerden kaynaklanmadığını, ancak flavonoid depolimerizasyonu ve atılımından kaynaklanan ürik asit üretiminden kaynaklandığını göstermektedir.[30]
Enflamasyon
Enflamasyon, kanser, kardiyovasküler bozukluklar, diabetes mellitus, ve çölyak hastalığı gibi sayısız lokal ve sistemik hastalığın olası bir kaynağı olarak gösterilmektedir.[31]
Ön çalışmalar flavonoidlerin anti-inflamatuar mekanizmaları reaktif oksijen veya azot bileşiklerini inhibe etme yetenekleri ile etkileyebileceğini göstermektedir.[32] Flavonoidlerin ayrıca siklooksijenaz, lipooksijenaz veya indüklenebilir nitrik oksit sentaz gibi serbest radikal üretimine katılan enzimlerin proenflamatuar aktivitesini inhibe ettiği[32][33] veya bir inme sonrasında bağışıklık hücrelerinde veya beyin hücrelerinde hücre içi sinyal yollarını modifiye ettiği görüşü önerilmiştir.[32][34]
Bir flavonoid sınıfı olan prosiyanidinlerin, ön araştırmada, araşidonik asit yolunun modülasyonu, gen transkripsiyonunun inhibisyonu, enflamatuar enzimlerin ekspresyonu ve aktivitesinin yanı sıra anti-enflamatuar aracıların salgılanmasını içeren anti-enflamatuar mekanizmalara sahip olduğu gösterilmiştir.[35]
Kanser
Flavonoid tüketimi ile kanserin önlenmesi/gelişmesi arasındaki ilişkiyi araştıran klinik çalışmalar, çoğu kanser türü için çelişkilidir, çünkü çoğu çalışma retrospektiftir ve küçük bir örnek boyutu kullanılmıştır.[36] İki belirgin istisna gastrik karsinom ve sigara ile ilişkili kanserlerdir. Diyetlerle flavonoid alımı, kadınlarda mide karsinomu riskinin azalmasıyla,[37] ve sigara içenlerde solunum yolu kanseri riskinin azalmasıyla ilişkilendirilmiştir.[38]
Kardiyovasküler hastalıklar
Diyetle alınan flavonoidlerden etkilenmesi muhtemel olan genel insan hastalıkları üzerinde en yoğun çalışılan, kardiyovasküler hastalık araştırmaları, hastalar veya hasta olmayan kişilerde incelenen aşağıdaki mekanizmaları ortaya koymuştur:[39][40][41][42][43]
- pıhtılaşmayı, trombüs oluşumunu veya trombosit agregasyonunu inhibe eder
- ateroskleroz riskini azaltır
- arteriyel kan basıncını ve hipertansiyon riskini azaltır
- kan damarı hücrelerinde oksidatif stresi azaltır
- vasküler inflamatuar mekanizmaları onarır
- endotel ve kılcal fonksiyonların iyileştirilmesi
- kan lipit seviyelerini düzenler
- karbonhidrat ve glikoz metabolizmasını düzenler
- yaşlanma mekanizmalarını düzenler
Antibakteriyel
Flavonoidlerin doğrudan antibakteriyel aktiviteye, antibiyotiklerle sinerjistik aktiviteye ve çok sayıda in vitro ve sınırlı sayıda in vivo çalışmada bakteriyel virülans faktörlerini baskılama yeteneğine sahip olduğu gösterilmiştir.[19][44] Dikkate değer in vivo çalışmalar arasında[45][46][47], oral kursetinin kobaylarda, grup 1 kanserojen Helicobacter pylori'ye karşı koruduğu bulgusudur.[47] Flavonoidlerin bakteriyel enfeksiyonun tedavisi için farmasötik ilaçlar olarak kullanılıp kullanılamayacağını veya diyet flavonoid alımının enfeksiyona karşı herhangi bir koruma sağlayıp sağlamadığını belirlemek için ek in vivo ve klinik araştırmalara ihtiyaç vardır.
Sentezi, tespiti, miktar tayini ve yarı sentetik alterasyonu
Renk tayfı
Bitkilerdeki flavonoid sentezi, hem yüksek hem de düşük enerji radyasyonlarında açık renk spektrumları ile indüklenir. Düşük enerjili radyasyonlar fitokrom tarafından soğurulurken, yüksek enerjili radyasyonlar fitokromlara ek olarak karotenoidler , flavinler ve kriptokromlar tarafından soğurulur. Fitokrom aracılı flavonoid biyosentezinin fotomorfojenik süreci amaranthus, arpa, mısır, sorgum ve şalgamda gözlenmiştir. Kırmızı ışık flavonoid sentezini arttırır.[48]
Mikroorganizmalardan eldesi
Son araştırmalar, genetik olarak tasarlanmış mikroorganizmalardan flavonoid moleküllerinin verimli bir şekilde üretilebildiği gösterilmiştir.[49][50][51]
Tespit testleri
- Shinoda testi
Dört parça magnezyum talaşı etanolik ekstrakta eklenir ve ardından birkaç damla doygun hidroklorik asit eklenir. Pembe veya kırmızı renk, flavonoidin varlığını gösterir.[52] Turuncudan kırmızıya değişen renkler flavonların varlığını, kırmızıdan koyu kırmızıya değişen renkler flavonoidlerin varlığını, koyu kırmızıdan macentaya değişen renkler flavononların varlığını gösterir.
- Sodyum hidroksit testi
Yaklaşık 5 mg bileşik su içinde çözülür, ısıtılır ve süzülür. Bu çözeltinin 2 ml'sine %10 sodyum hidroksit eklenir. Sarı bir renk oluşur. Seyreltik hidroklorik asit ilavesiyle sarı rengin kaybolması ve çözeltinin renksizleşmesi, flavonoidlerin varlığının bir göstergesidir.[53]
- p-Dimetilaminokinnamaldehit testi
Biradaki flavanoidler için, A-halkalarının kromojen p-dimetilaminosinnamaldehit (DMACA) ile reaksiyonuna dayanan kolorimetrik bir analiz geliştirilmiştir.[54]
Miktar tayini
Lamaison ve Carnet, bir numunenin toplam flavonoid içeriğinin belirlenmesi için bir test tasarlamıştır (AlCI3 yöntemi). Numunenin ve reaktifin uygun şekilde karıştırılmasından sonra, karışım 10 dakika oda sıcaklığında inkübe edilir ve çözeltinin absorbans değeri 440 nm'de okunur. Flavonoid içeriği, mg/g kuersetin olarak ifade edilir.[55]
Yarı sentetik alterasyonu
İmmobilize Candida antarktika lipazı, flavonoidlerin regioselektif asilasyonunu katalize etmek için kullanılabilir.[56]
Ayrıca bakınız
- Fitokimyasallar
- Fitokimya
- Sekonder metabolitler
- Homoizoflavonoidler
Kaynakça
- McNaught, Alan D; Wilkinson, Andrew; IUPAC (1997), IUPAC Compendium of Chemical Terminology (2 bas.), Oxford: Blackwell Scientific, doi:10.1351/goldbook.F02424, ISBN 978-0-9678550-9-7
- "Flavonoids (isoflavonoids and neoflavonoids)", The Gold Book, 2009, doi:10.1351/goldbook, ISBN 978-0-9678550-9-7, erişim tarihi: 16 Eylül 2012 Geçersiz
|mod=cs1(yardım) - Galeotti, F; Barile, E; Curir, P; Dolci, M; Lanzotti, V (2008). "Flavonoids from carnation (Dianthus caryophyllus) and their antifungal activity". Phytochemistry Letters. Cilt 1. ss. 44-48. doi:10.1016/j.phytol.2007.10.001.
- Ververidis F, Trantas E, Douglas C, Vollmer G, Kretzschmar G, Panopoulos N (Ekim 2007). "Biotechnology of flavonoids and other phenylpropanoid-derived natural products. Part I: Chemical diversity, impacts on plant biology and human health". Biotechnology Journal. 2 (10). ss. 1214-34. doi:10.1002/biot.200700084. PMID 17935117.
- Isolation of a UDP-glucose: Flavonoid 5-O-glucosyltransferase gene and expression analysis of anthocyanin biosynthetic genes in herbaceous peony (Paeonia lactiflora Pall.). Da Qiu Zhao, Chen Xia Han, Jin Tao Ge and Jun Tao, Electronic Journal of Biotechnology, 15 November 2012, Volume 15, Number 6, DOI:10.2225/vol15-issue6-fulltext-7
- Spencer JP (2008). "Flavonoids: modulators of brain function?". British Journal of Nutrition. 99 (E-S1). ss. ES60-77. doi:10.1017/S0007114508965776. PMID 18503736.
- Oomah, B. Dave; Mazza, Giuseppe (1996). "Flavonoids and Antioxidative Activities in Buckwheat". Journal of Agricultural and Food Chemistry. 44 (7). ss. 1746-1750. doi:10.1021/jf9508357.
- Ayoub M, de Camargo AC, Shahidi F (2016). "Antioxidants and bioactivities of free, esterified and insoluble-bound phenolics from berry seed meals". Food Chemistry. 197 (Part A). ss. 221-232. doi:10.1016/j.foodchem.2015.10.107. PMID 26616944.
- The Lancet (2007). "The devil in the dark chocolate". Lancet. 370 (9605). s. 2070. doi:10.1016/S0140-6736(07)61873-X. PMID 18156011.
- de Camargo AC, Regitano-d'Arce MA, Gallo CR, Shahidi F (2015). "Gamma-irradiation induced changes in microbiological status, phenolic profile and antioxidant activity of peanut skin". Journal of Functional Foods. Cilt 12. ss. 129-143. doi:10.1016/j.jff.2014.10.034.
- Chukwumah Y, Walker LT, Verghese M (2009). "Peanut skin color: a biomarker for total polyphenolic content and antioxidative capacities of peanut cultivars". Int J Mol Sci. 10 (11). ss. 4941-52. doi:10.3390/ijms10114941. PMC 2808014 $2. PMID 20087468.
- "Flavonoids - Linus Pauling Institute - Oregon State University". 28 Nisan 2014. 24 Ekim 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Şubat 2016.
- "FDA approved drug products". US Food and Drug Administration. 23 Ocak 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Kasım 2013.
- "Health Claims Meeting Significant Scientific Agreement". US Food and Drug Administration. 14 Kasım 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Kasım 2013.
- EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA) (2010). "Scientific Opinion on the substantiation of health claims related to various food(s)/food constituent(s) and protection of cells from premature aging, antioxidant activity, antioxidant content and antioxidant properties, and protection of DNA, proteins and lipids from oxidative damage pursuant to Article 13(1) of Regulation (EC) No 1924/20061". EFSA Journal. 8 (2). s. 1489. doi:10.2903/j.efsa.2010.1489.
- Yamamoto Y, Gaynor RB (2001). "Therapeutic potential of inhibition of the NF-κB pathway in the treatment of inflammation and cancer". Journal of Clinical Investigation. 107 (2). ss. 135-42. doi:10.1172/JCI11914. PMC 199180 $2. PMID 11160126.
- Cazarolli LH, Zanatta L, Alberton EH, Figueiredo MS, Folador P, Damazio RG, Pizzolatti MG, Silva FR (2008). "Flavonoids: Prospective Drug Candidates". Mini-Reviews in Medicinal Chemistry. 8 (13). ss. 1429-1440. doi:10.2174/138955708786369564. PMID 18991758.
- Cushnie TP, Lamb AJ (2011). "Recent advances in understanding the antibacterial properties of flavonoids". International Journal of Antimicrobial Agents. 38 (2). ss. 99-107. doi:10.1016/j.ijantimicag.2011.02.014. PMID 21514796. 26 Temmuz 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Manner S, Skogman M, Goeres D, Vuorela P, Fallarero A (2013). "Systematic exploration of natural and synthetic flavonoids for the inhibition of Staphylococcus aureus biofilms". International Journal of Molecular Sciences. 14 (10). ss. 19434-19451. doi:10.3390/ijms141019434. PMC 3821565 $2. PMID 24071942.
- Cushnie TP, Lamb AJ (2005). "Antimicrobial activity of flavonoids" (PDF). International Journal of Antimicrobial Agents. 26 (5). ss. 343-356. doi:10.1016/j.ijantimicag.2005.09.002. PMID 16323269. 8 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Friedman M (2007). "Overview of antibacterial, antitoxin, antiviral, and antifungal activities of tea flavonoids and teas". Molecular Nutrition & Food Research. 51 (1). ss. 116-134. doi:10.1002/mnfr.200600173. PMID 17195249.
- de Sousa RR, Queiroz KC, Souza AC, Gurgueira SA, Augusto AC, Miranda MA, Peppelenbosch MP, Ferreira CV, Aoyama H (2007). "Phosphoprotein levels, MAPK activities and NFkappaB expression are affected by fisetin". J Enzyme Inhib Med Chem. 22 (4). ss. 439-444. doi:10.1080/14756360601162063. PMID 17847710.
- Schuier M, Sies H, Illek B, Fischer H (2005). "Cocoa-related flavonoids inhibit CFTR-mediated chloride transport across T84 human colon epithelia". J. Nutr. 135 (10). ss. 2320-5. doi:10.1093/jn/135.10.2320. PMID 16177189. 18 Mayıs 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Esselen M, Fritz J, Hutter M, Marko D (2009). "Delphinidin Modulates the DNA-Damaging Properties of Topoisomerase II Poisons". Chemical Research in Toxicology. 22 (3). ss. 554-64. doi:10.1021/tx800293v. PMID 19182879.
- Bandele OJ, Clawson SJ, Osheroff N (2008). "Dietary polyphenols as topoisomerase II poisons: B-ring substituents determine the mechanism of enzyme-mediated DNA cleavage enhancement". Chemical Research in Toxicology. 21 (6). ss. 1253-1260. doi:10.1021/tx8000785. PMC 2737509 $2. PMID 18461976.
- Barjesteh van Waalwijk van Doorn-Khosrovani S, Janssen J, Maas LM, Godschalk RW, Nijhuis JG, van Schooten FJ (2007). "Dietary flavonoids induce MLL translocations in primary human CD34+ cells". Carcinogenesis. 28 (8). ss. 1703-9. doi:10.1093/carcin/bgm102. PMID 17468513.
- Lotito SB, Frei B (2006). "Consumption of flavonoid-rich foods and increased plasma antioxidant capacity in humans: cause, consequence, or epiphenomenon?". Free Radic. Biol. Med. 41 (12). ss. 1727-46. doi:10.1016/j.freeradbiomed.2006.04.033. PMID 17157175.
- Williams RJ, Spencer JP, Rice-Evans C (2004). "Flavonoids: antioxidants or signalling molecules?". Free Radical Biology & Medicine. 36 (7). ss. 838-49. doi:10.1016/j.freeradbiomed.2004.01.001. PMID 15019969.
- Stauth D (5 Mart 2007). "Studies force new view on biology of flavonoids". EurekAlert!, Adapted from a news release issued by Oregon State University. 4 Aralık 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Ferretti G, Bacchetti T, Masciangelo S, Saturni L (2012). "Celiac Disease, Inflammation and Oxidative Damage: A Nutrigenetic Approach". Nutrients. 4 (12). ss. 243-257. doi:10.3390/nu4040243. PMC 3347005 $2. PMID 22606367.
- Izzi V, Masuelli L, Tresoldi I, Sacchetti P, Modesti A, Galvano F, Bei R (2012). "The effects of dietary flavonoids on the regulation of redox inflammatory networks". Frontiers in Bioscience. 17 (7). ss. 2396-2418. doi:10.2741/4061. PMID 22652788.
- Gomes A, Couto D, Alves A, Dias I, Freitas M, Porto G, Duarte JA, Fernandes E (2012). "Trihydroxyflavones with antioxidant and anti-inflammatory efficacy". BioFactors. 38 (5). ss. 378-386. doi:10.1002/biof.1033. PMID 22806885.
- Chang CF, Cho S, Wang J (Apr 2014). "(-)-Epicatechin protects hemorrhagic brain via synergistic Nrf2 pathways". Ann Clin Transl Neurol. 1 (4). ss. 258-271. doi:10.1002/acn3.54. PMC 3984761 $2. PMID 24741667.
- Martinez-Micaelo N, González-Abuín N, Ardèvol A, Pinent M, Blay MT (2012). "Procyanidins and inflammation: Molecular targets and health implications". BioFactors. 38 (4). ss. 257-265. doi:10.1002/biof.1019. PMID 22505223.
- Romagnolo DF, Selmin OI (2012). "Flavonoids and cancer prevention: a review of the evidence". J Nutr Gerontol Geriatr. 31 (3). ss. 206-38. doi:10.1080/21551197.2012.702534. PMID 22888839.
- González CA, Sala N, Rokkas T (2013). "Gastric cancer: epidemiologic aspects". Helicobacter. 18 (Supplement 1). ss. 34-38. doi:10.1111/hel.12082. PMID 24011243.
- Woo HD, Kim J (2013). "Dietary flavonoid intake and smoking-related cancer risk: a meta-analysis". PLoS ONE. 8 (9). ss. e75604. Bibcode:2013PLoSO...875604W. doi:10.1371/journal.pone.0075604. PMC 3777962 $2. PMID 24069431.
- Higdon, J; Drake, V; Frei, B (Mart 2009). "Non-Antioxidant Roles for Dietary Flavonoids: Reviewing the relevance to cancer and cardiovascular diseases". Nutraceuticals World. Rodman Media. 21 Aralık 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 24 Kasım 2013.
- van Dam RM, Naidoo N, Landberg R (2013). "Dietary flavonoids and the development of type 2 diabetes and cardiovascular diseases". Current Opinion in Lipidology. 24 (1). ss. 25-33. doi:10.1097/MOL.0b013e32835bcdff. PMID 23254472.
- Tangney CC, Rasmussen HE (2013). "Polyphenols, Inflammation, and Cardiovascular Disease". Current Atherosclerosis Reports. 15 (5). s. 324. doi:10.1007/s11883-013-0324-x. PMC 3651847 $2. PMID 23512608.
- Siasos G, Tousoulis D, Tsigkou V, Kokkou E, Oikonomou E, Vavuranakis M, Basdra EK, Papavassiliou AG, Stefanadis C (2013). "Flavonoids in atherosclerosis: An overview of their mechanisms of action". Current Medicinal Chemistry. 20 (21). ss. 2641-2660. doi:10.2174/0929867311320210003. PMID 23627935.
- Cappello, AR, Dolce V, Iacopetta D, Martello M, Fiorillo M, Curcio R, Muto L, Dhanyalayam D. (2015). "Bergamot (Citrus bergamia Risso) Flavonoids and Their Potential Benefits in Human Hyperlipidemia and Atherosclerosis: an Overview". Mini-Reviews in Medicinal Chemistry. 16 (8). ss. 1-11. doi:10.2174/1389557515666150709110222. PMID 26156545.
- Taylor PW, Hamilton-Miller JM, Stapleton PD (2005). "Antimicrobial properties of green tea catechins". Food Science and Technology Bulletin. 2 (7). ss. 71-81. doi:10.1616/1476-2137.14184. PMC 2763290 $2. PMID 19844590.
- Choi O, Yahiro K, Morinaga N, Miyazaki M, Noda M (2007). "Inhibitory effects of various plant polyphenols on the toxicity of Staphylococcal alpha-toxin". Microbial Pathogenesis. 42 (5–6). ss. 215-224. doi:10.1016/j.micpath.2007.01.007. PMID 17391908.
- Oh DR, Kim JR, Kim YR (2010). "Genistein inhibits Vibrio vulnificus adhesion and cytotoxicity to HeLa cells". Archives of Pharmacal Research. 33 (5). ss. 787-792. doi:10.1007/s12272-010-0520-y. PMID 20512479.
- González-Segovia R, Quintanar JL, Salinas E, Ceballos-Salazar R, Aviles-Jiménez F, Torres-López J (2008). "Effect of the flavonoid quercetin on inflammation and lipid peroxidation induced by Helicobacter pylori in gastric mucosa of guinea pig". Journal of Gastroenterology. 43 (6). ss. 441-447. doi:10.1007/s00535-008-2184-7. PMID 18600388.
- Sinha, Rajiv Kumar (1 Ocak 2004). Modern Plant Physiology (İngilizce). CRC Press. s. 457. ISBN 9780849317149. 10 Nisan 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Hwang EI, Kaneko M, Ohnishi Y, Horinouchi S (Mayıs 2003). "Production of plant-specific flavanones by Escherichia coli containing an artificial gene cluster". Appl. Environ. Microbiol. 69 (5). ss. 2699-706. doi:10.1128/AEM.69.5.2699-2706.2003. PMC 154558 $2. PMID 12732539.
- Trantas E, Panopoulos N, Ververidis F (2009). "Metabolic engineering of the complete pathway leading to heterologous biosynthesis of various flavonoids and stilbenoids in Saccharomyces cerevisiae". Metabolic Engineering. 11 (6). ss. 355-366. doi:10.1016/j.ymben.2009.07.004. PMID 19631278.
- Ververidis F, Trantas E, Douglas C, Vollmer G, Kretzschmar G, Panopoulos N (2007). "Biotechnology of flavonoids and other phenylpropanoid-derived natural products. Part II: Reconstruction of multienzyme pathways in plants and microbes". Biotechnology Journal. 2 (10). ss. 1235-49. doi:10.1002/biot.200700184. PMID 17935118.
- Yisa, Jonathan (2009). "Phytochemical Analysis and Antimicrobial Activity Of Scoparia Dulcis and Nymphaea Lotus". Australian Journal of Basic and Applied Sciences. 3 (4). ss. 3975-3979. 17 Ekim 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Ocak 2020.
- Bello IA, Ndukwe GI, Audu OT, Habila JD (2011). "A bioactive flavonoid from Pavetta crassipes K. Schum". Organic and Medicinal Chemistry Letters. 1 (1). s. 14. doi:10.1186/2191-2858-1-14. PMC 3305906 $2. PMID 22373191.
- A new colourimetric assay for flavonoids in pilsner beers. Jan A. Delcour and Didier Janssens de Varebeke, Journal of the Institute of Brewing, January–February 1985, Volume 91, Issue 1, pages 37–40, DOI:10.1002/j.2050-0416.1985.tb04303.x
- Lamaison, JL; Carnet, A (1991). "Teneurs en principaux flavonoides des fleurs de Cratageus monogyna Jacq et de Cratageus Laevigata (Poiret D.C) en Fonction de la vegetation". Plantes Medicinales Phytotherapie. Cilt 25. ss. 12-16.
- Passicos E, Santarelli X, Coulon D (2004). "Regioselective acylation of flavonoids catalyzed by immobilized Candida antarctica lipase under reduced pressure". Biotechnol. Lett. 26 (13). ss. 1073-1076. doi:10.1023/B:BILE.0000032967.23282.15. PMID 15218382.
Konuyla ilgili yayınlar
- Andersen, Ø.M. / Markham, K.R. (2006). Flavonoids: Chemistry, Biochemistry and Applications. CRC Press. 978-0-8493-2021-7
- Grotewold, Erich (2007). The Science of Flavonoids. Springer. 978-0-387-74550-3
- Comparative Biochemistry of the Flavonoids, by J.B. Harborne, 1967 (Google Books 1 Ağustos 2020 tarihinde Wayback Machine sitesinde arşivlendi.)
- The systematic identification of flavonoids, by T.J. Mabry, K.R. Markham and M.B. Thomas, 1970, DOI:10.1016/0022-2860(71)87109-0
| Wikimedia Commons'ta Flavonoids ile ilgili ortam dosyaları bulunmaktadır. |
