Asetik asit
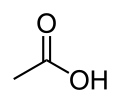
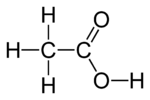
Asetik asit veya etanoik asit CH3COOH formüllü bir organik asittir, sirkeye ekşi tadını ve keskin kokusunu vermesiyle bilinir. Karboksilik asitlerin en küçüklerindendir (en küçük olan formik asittir). Doğada karbonhidratların yükseltgenmesiyle oluşur. Sanayide asetik asit hem biyolojik yolla hem de sentetik yolla imal edilir. Tuz ve esterine asetat denir. Suda tamamen çözünür.
| Asetik asit | |
|---|---|
 | |
 | |
 | |
 | |
 | |
Etanoik asit | |
| Tanımlayıcılar | |
| Kısaltmalar | AcOH |
| CAS numarası | 64-19-7 |
| PubChem | 176 |
| EC numarası | 200-580-7 |
| UN numarası | 2789 |
| DrugBank | DB03166 |
| KEGG | D00010 |
| MeSH | Acetic+acid |
| ChEBI | 15366 |
| RTECS numarası | AF1225000 |
| SMILES |
|
| Beilstein | 506007 |
| Gmelin veritabanı | 1380 |
| ChemSpider | 171 |
| 3DMet | B00009 |
| Özellikler | |
| Kimyasal formül | C2H4O2 |
| Molekül kütlesi | 60,05 g mol−1 |
| Görünüm | Renksiz sıvı |
| Koku | Keskin, sirke gibi |
| Yoğunluk | 1.049 g cm−3 |
| Erime noktası |
16-17 °C; 61-62 °F; 289-290 K |
| Kaynama noktası |
118-119 °C; 244-246 °F; 391-392 K |
| Çözünürlük (su içinde) | Karışabilir. |
| log P | -0.322 |
| Asitlik (pKa) | 4.76[5] |
| Baziklik (pKb) | 9.24 (Asetat iyonunun bazikliği) |
| Tehlikeler | |
| NFPA 704 |
 2
3
0
|
| Parlama noktası | 40 °C (104 °F; 313 K) |
| Öztutuşma sıcaklığı |
427 °C (801 °F; 700 K) |
| Patlama sınırları | 4–16% |
| ABD maruz kalma limiti (PEL) |
TWA 10 ppm (25 mg/m³) |
| LD50 | 3.31 g kg−1, oral (sıçan) |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Kullanımı
Sirke
Sirke genelde %4-5 oranında asetik asit içerir ama turşu kurmak için kullanılan sirkelerde bu oran %18'e varır. Sirkenin oluşturduğu asitli ortam gıdaların bozulmasına neden olacak çoğu mikroorganizmanın büyümesini engeller. Bu yüzden turşulama sebzelerin ömrünü uzatmak için etkili bir yöntemdir.
Sanayi

Sanayide asetik asitin geniş bir kullanım alanı vardır, çoğu kimyasalın üretiminde hammadde olarak kullanılır. En önemli kullanımı vinil asetat üretimidir ve bundan elde edilen polivinil asetat tahta tutkalı olarak kullanılır. Bunu asetik anhidrit ve asetik ester üretimi izler. Sirke üretiminde kullanımı nispeten önemsizdir. Asetik asitin bir diğer önemli kullanımı çözücü olaraktır. PET plastiklerin üretiminde kullanılan tereftalik asit üretiminde asetik asit çözücü olarak kullanılır, bu kullanım asetik asitin tüm kullanımının %5-10'unu oluşturur. Asetik asit gıda sanayisinden tampon özelliğinden dolayı E260 adıyla bir katkı maddesi olarak kullanılır.
Asetik asidin türevlerinin de çeşitli kullanımları vardır. Örneğin, Sodyum asetat dokuma sanayinde ve gıda katkı maddesi olarak (E262) kullanılır. Selüloz asetat fotoğraf filmi üretiminde kullanılır.
Asetik asidin zayıf bir asit olması onun özellikle ev içinde temizleme amacıyla kullanılmasının nedenidir. Seyreltik asetik asit (sirke) çaydanlıkların kireçten arındırılmasında, cam ve diğer parlak yüzeylerdeki madenî birikmeleri temizlemekte kullanılabilir.
Etkileri

Yoğun asetik asit cildi yakar, göze kalıcı zarar verir ve ciltte kabarcıklar oluşmasına neden olur. Etkileri birkaç saat sonra hissedilir. Bu etkilerden korunmak için nitril koruma eldivenleri giyilir. Asetik asit 39 °C üzerinde tutuşabilir, havayla patlayıcı karışımlar oluşturabilir.
%25'den daha yoğun asetik asit labarutuarlarda çekerocak altında kullanılmalıdır. Seyreltik asetik asit zararsızdır, ama daha kuvvetli çözeltileri insan ve hayvanlar için zararlıdır. Sindirim sistemine ciddi hasar verebilir ve kan asitliğini ölümcül oranda değiştirebilir.
Kaynakça
- IUPAC, Commission on Nomenclature of Organic Chemistry (1993). "Table 28(a) Carboxylic acids and related groups. Unsubstituted parent structures". A Guide to IUPAC Nomenclature of Organic Compounds (Recommendations 1993). Blackwell Scientific publications. ISBN 0-632-03488-2. 25 Nisan 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2016.
- "Acetic Acid – PubChem Public Chemical Database". The PubChem Project. ABD: National Center for Biotechnology Information. 14 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2016.
- Scientific literature reviews on generally recognised as safe (GRAS) food ingredients. National Technical Information Service. 1974. s. 1.
- "Chemistry", volume 5, Encyclopedia Britannica, 1961, page 374
- Ripin, D. H.; Evans, D. A. (4 Kasım 2005). "pKa Table" (PDF). 22 Temmuz 2015 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 19 Temmuz 2015.
