Aktinyum(III) oksit
Aktinyum(III) oksit, az görülen radyoaktif element olan aktinyumun metalik oksitlenmesiyle oluşan bir bileşiktir. Aktinyum(III) oksitin formülü Ac2O3'tür. Bu oksit aktinyum oksalatın 1000-1100 derecede kızdırılmasıyla elde edilir.[2] Lantan(III) oksit ile benzerlik gösterir. Hegzagonal ve kristal bir yapıya sahiptir. Yükseltgenme seviyesi +3'tür.[3][4] Yoğunluğu 9.2g/ml, erime noktası 1977 °C dir. Görünümü beyazdır. Bu element Ac2O (Asetik anhidrit) ile karışmamalıdır. Buradaki Ac asetil grubunda bulunmaktadır. Diğer adları aktinyum seskioksit ile diaktinyum trioksittir.
| Aktinyum(III) oksit | |
|---|---|
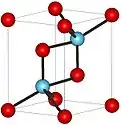 | |
Aktinyum(III) oksit | |
Aktinyum(3+) oksit | |
Diğer adlar Aktinyum seskioksit, diaktinyum trioksit | |
| Tanımlayıcılar | |
| CAS numarası | 12002-61-8 |
| PubChem | 21946271 |
| SMILES |
|
| Özellikler | |
| Molekül formülü | Ac2O3 |
| Molekül kütlesi | 502.053 g/mol[1] |
| Görünüm | Beyaz |
| Yoğunluk | 9.2 g/ml |
| Erime noktası |
1977 °C |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Tepkimeleri
Bazı bulunduğu tepkimeler:
- Ac2O3 + 6HF → 2AcF3 + 3H2O
- Ac2O3 + 6HCl → 2AcCl3 + 3H2O
- 4Ac(NO3)3 → 2Ac2O3 + 12NO2 + 3O2
- 4Ac + 3O2 → 2Ac2O3
- Ac2O3 + 2AlBr3 → 2AcBr3 + Al2O3
- 2Ac(OH)3 → Ac2O3 + 3H2O
- Ac2(C2O4)3 → Ac2O3 + 3CO2 + 3CO
- Ac2O3 + H2S → Ac2S3 + 3H2O
Aliminyum bromür ile aktinyum oksit reaksiyonunda ürünlerden aktinyum tribromür[4]:
- Ac2O3 + 2 AlBr3 → 2 AcBr3 + Al2O3
Aktinyumun metal ile oksitlenmesiyle aktinyum(III) oksit oluşuyor ve daha sonra bu maddenin sentezi için kullanılıyor[5]:
- 4Ac + 3O2 → 2Ac2O3
- Ac2O3 + H2S → Ac2S3 + 3H2O
Aktinyum oksalatın 1000-1100 derecede kızdırılmasıyla aktinyum(III) oksit elde edilir[2]:
- Ac2(C2O4)3 → Ac2O3 + 3CO2 + 3CO
Aktinyum(III) oksit ile hidrojen florürün 700 °C sıcaklıkta tepkimeye girince aktinyum(III) florür ile su oluşuyor[6]:
- Ac2O3 + 6HF → 2AcF3 + 3H2O
Aktinyum(III) oksit ile hidroklorik asit tepkimeye girince ortaya aktinyum(III) klorür ile su oluşuyor[7]:
- Ac2O3 + 6HCl → 2AcCl3 + 3H2O
Aktinyum(III) hidroksil, aktinyum(III) oksit ile suya dönüşüyor. Bu reaksiyon 1100 °C civarlarında[8] gerçekleştirilmektedir:
- 2Ac(OH)3 → Ac2O3 + 3H2O
Aktinyum(III) nitrat; aktinyum(III) oksit, azot dioksit ve oksijene dönüşüyor. Bu reaksiyon 600 °C ile 800 °C sıcaklıkları arasında gerçekleşmektedir[9]:
- 4Ac(NO3)3 → 2Ac2O3 + 12NO2 + 3O2
Kaynakça
- PubChem Diactinium Trioxide
- Aktinyumun Bileşikleri (Türkçe)
- Aktinyum 14 Aralık 2013 tarihinde Wayback Machine sitesinde arşivlendi. Büyük Sovyet Ansiklopedisi (Rusça)
- PUBS (İngilizce)
- Slidegur
- Chemiday 3-1-0-2087
- Chemiday 3-1-0-2086
- Chemiday 3-1-0-2093
- Chemiday 3-1-0-2079
